

个人信息
Personal Information
联系方式
Contact Information
个人简介
Personal Profile
谢敬教授:现任同济大学-生命科学与技术学院教授、博士生导师。中组部海外高层次人才计划入选者。
2010获中国科学院-上海生物化学与细胞生物学研究所(SIBCB, CAS)博士学位。2012年起于美国约翰.霍普金斯大学(Johns Hopkins University, JHU)从事博士后研究。导师为JHU终身教授,霍华德休斯(HHMI)研究员Xin Chen教授。研究期间与包括诺贝尔奖得主 Prof.Eric Betzig 在内多位世界一流的科学家开展合作,将超高分辨率显微成像技术(Superresolution imaging),单分子分析(Singlemolecule analysis) 等前沿技术应用于自己的研究中。
主要论著发表在包括《Cell》, 《Science》,《Cell Discovery》和《Trends in Cell Biology》等国际著名学术期刊上,并获得多项美国及中国发明专利。研究成果获领域内同行的认可和好评,包括《Cell》,《Nature Reviews Molecular Cell Biology》, 《Nature Reviews Genetics》 和 Faculty 1000 Prime 等诸多国际知名学术期刊和平台对这些研究成果进行了重点评述和推荐。
本课题组正招聘助理教授,博士后和研究助理。欢迎博士生,硕士生,本科生报考和实习。具体事宜可先通过Email联系。


课题组受到“科技部”、“国家自然基金委”等机构资助,主持/承担多个科学研究项目。
上传附件
支持扩展名:.rar .zip .doc .docx .pdf .jpg .png .jpeg上传附件
支持扩展名:.rar .zip .doc .docx .pdf .jpg .png .jpeg上传附件
支持扩展名:.rar .zip .doc .docx .pdf .jpg .png .jpeg非对称分裂(ACD)是被胚胎干细胞以及多种成体干细胞所广泛采用的一种特殊的细胞分裂形式。通过一次ACD,干细胞将产生两个具有不同细胞命运的子细胞:其中一个保留干细胞的特性,成为新一代干细胞,以维持干细胞总数的动态平衡;而另一个子细胞则会失去干细胞特性,进入定向分化,为组织的发育提供细胞的物质基础。由此可见,干细胞通过ACD将分裂增殖与分化发育两大基本生理活动相互耦合在一个生物学过程中。
ACD是一个必须受到极其严格调控的生物学过程(即控制两种不同类型子细胞之间的动态平衡至关重要),因为一旦失衡,就可能会出现干细胞过度增殖,或者干细胞丢失两种相反的极端现象,从而会导致威胁人类健康的两类主要疾病:肿瘤发生和组织退化。
课题组受到“科技部”、“国家自然基金委”等机构资助,主持/承担多个科学研究项目。
本实验室关注于以下两方面的问题的研究:
1) 干细胞表观遗传记忆的跨代传递机制
聚焦胚胎发育与干细胞分化中组蛋白修饰的动态重编程,解析表观遗传信息如何跨代传递并调控子细胞命运。为干细胞治疗中的定向诱导分化策略提供理论支撑,助力再生医学优化。
2) 单分子尺度基因转录动态与命运决定
开发MS2/MCP标记系统与超分辨成像联用技术,解析基因转录实时动态如何影响细胞命运决策。突破传统群体平均分析的局限,揭示单细胞异质性机制。
3) 组蛋白突变驱动的病理机制研究
结合单细胞多组学与活细胞成像,揭示突变导致染色质异常开放/压缩的分子路径,实现突变效应时空追踪,阐明其在组织退化(如衰老)与肿瘤发生中的作用。
4) 干细胞的临床转化研究
结合基因编辑,活细胞超分辨率成像,多组学数据分析等技术手段,评估干细胞对组织再生的效果,并深入探索干细胞生理环境下参与组织修复的分子机制。
本实验室综合利用哺乳动物胚胎干细胞及小鼠等模型,探索基于组蛋白的表观遗传调控机制对于干性/分化基因表达状态,干细胞维持以及细胞谱系发育等生物学过程的影响。目前实验室已搭建了特色的技术平台,助力于研究工作的开展;并对以干细胞定向诱导分化为主线的再生医学发展产生直接的临床指导作用。
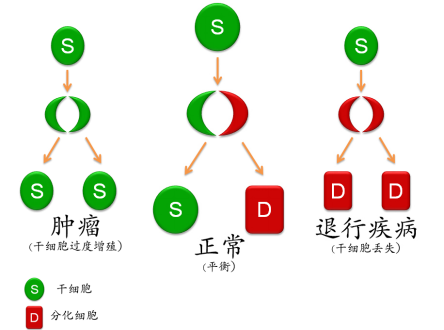
干细胞非对称分裂与人类主要疾病的关系
(In reverse chronological order)
1.Xie, J.*, Wooten, M.*, Tran, V. and Chen, X. (2017) Breaking Symmetry—Asymmetry Histone Inheritance in Stem Cells, Trends in Cell Biology, 27( 7), 527-40. * co-first authors
2.Xie J., Wooten M., Tran V., Chen BZ., Pozmanter C., Simbolon C., Betzig E. and Chen X., (2015). Histone H3 Threonine 3 Phosphorylation Regulates Asymmetric Histone Inheritance in the in Drosophila Male Germline. Cell. 163(4):920-33.
(Previewed by Pirrotta, V. (2015) Histone Marks Direct Chromosome Segregation. Cell. 163(4): 792–793. Highlighted by Strzyz, P. (2015) Stem cells: Histone Mark of Stemness. Nat Rev Mol Cell Biol. 16(12):703. Featured in Faculty of 1000 Prime.)
3.Du AY. *, Xie J. *, Guo KJ., Wan YH., Yang Lei., Niu X., Wu J., Dong XQ., and Zhang XJ. (2015). A Novel Function of Acetylcholinesterase: AChE Plays as a DNase that Degrades DNA during Apoptosis. Cell Discovery 1, 15002 * co-first authors (Highlighted by Sánchez-Osuna, M. and Yuste, V. (2015) AChE for DNA Degradation. Cell Research 25:653–654.)
4.Tran V.*, Lim C.*, Xie J. and Chen X. (2012) Asymmetric Division of Drosophila Male Germline Stem Cell Shows Asymmetric Histone Distribution. Science. 338, 679-682 * co-first authors
(Highlighted by Muers, M (2012) Epigenetics: Asymmetric histone distribution in stem cells. Nature Reviews Genetics 13:827. Featured in Faculty of 1000 Prime.)
5.Niu X., Zhang XJ., Xie J. and Zhang XJ. (2012). Acetylcholinesterase Blocks Cleavage of APP by γ-secretase in 293 Cells and Mouse Brain. Molecular Neurodegeneration. 7(Suppl 1): S11.
6.Xie J.,Jiang H., Wan YH., Du AY., Guo KJ., Liu T., Ye WY., Niu X., Wu J., Dong XQ., and Zhang XJ. (2011). Induction of a 55 kDa Acetylcholinesterase (AChE) Protein during Apoptosis and its Negative Regulation by the Akt Pathway. Journal of Molecular Cell Biology. 3(4), 250-259.
7.Ye WY.*, Gong XW.*, Xie J., Wu J., Zhang XJ., Ouyang Q., Shi YF., and Zhang XJ. (2010). AChE Deficiency or Inhibition Decreases Apoptosis and p53 Expression and Protects Renal Function after Ischemia/Reperfusion. Apoptosis. 15, 474-487. * co-first authors
8.Xiang AC., Xie J., and Zhang XJ. (2008). Acetylcholinesterase in Intestinal Cell Differentiation involves G2/M Cell Cycle Arrest. Cellular and Molecular Life Sciences. 65, 1768-1779.
9. Wu JC., LiuTJ., Xie J., Xin F., and Guo LH. (2006). Mitochondria and Calpains Mediate Caspase-Dependent Apoptosis Induced by Doxycycline in HeLa Cells. Cellular and Molecular Life Sciences. 63, 949-957.
本课题组正招聘助理教授,博士后和研究助理。欢迎博士生,硕士生,本科生报考和实习。具体事宜可先通过Email联系。



文件上传中...